A.2.3. Passieve Transport Systemen (door de cel membraan)
Pagina Inhoud:
1.
Om een cel te laten leven, moet er communicatie (= transport) zijn tussen de extracellulaire vloeistof (= interstitiële vloeistof) en de intracellulaire vloeistof (= het cytoplasma).
2.
Sommige van deze transporten zijn passief en vereisen geen energie. Andere transportsystemen zijn ingewikkelder en vereisen energie (= ATP).
3.
Dit zijn de vier belangrijkste passieve transportsystemen:
- diffusie
- gefaciliteerde diffusie
- osmose
- filtratie
4.
Dit zijn de drie belangrijkste actieve transportsystemen:
- pompen (co-transporters, etc.)
- exocytose / endocytose
- fagocytose
1.
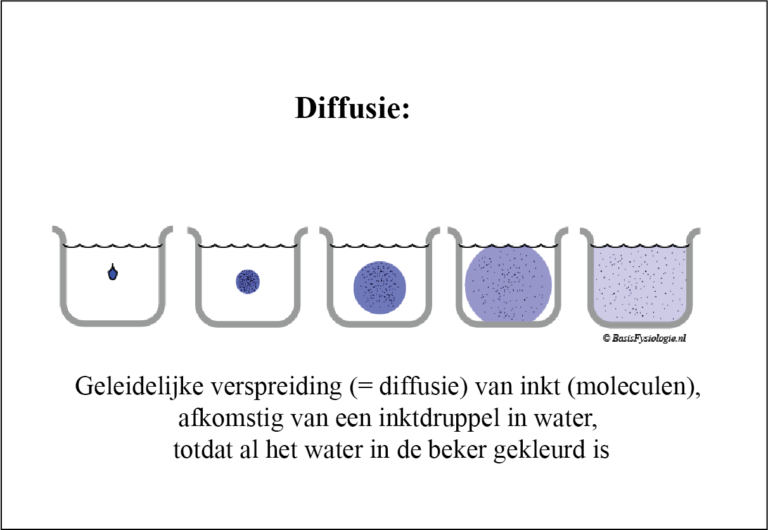
Diffusie is het proces waarbij iets oplosbaar dat in water wordt geplaatst ‘automatisch’ wordt verdeeld, opgelost, in dat water.
Diffusie is het proces waarbij iets oplosbaar dat in water wordt geplaatst ‘automatisch’ wordt verdeeld, opgelost, in dat water.
2.
Het klassieke voorbeeld is een druppel inkt dat in een glas water wordt gedruppeld. Als je lang genoeg wacht, wordt de inkt door het water verspreid.
Het klassieke voorbeeld is een druppel inkt dat in een glas water wordt gedruppeld. Als je lang genoeg wacht, wordt de inkt door het water verspreid.
3.
Hetzelfde geldt voor suiker, aspirine, zuurstof etc. zolang dit materiaal kan worden opgelost in water. Als het niet kan worden opgelost, dan zal diffusie natuurlijk niet plaatsvinden.
4.
Diffusie vindt plaats vanwege de Brownse bewegingen van de deeltjes. (Brownse bewegingen worden veroorzaakt door de kinetische energie die in elk deeltje is opgeslagen).(Wat is kinetisch?)
1.
In het lichaam vindt diffusie altijd plaats door de celmembranen. Dit gebeurt als de concentratie van iets (= de opgeloste stof) aan de ene kant van het membraan hoger is dan aan de andere kant, en als het membraan daarvoor doorlaatbaar is (= permeabel).
2.
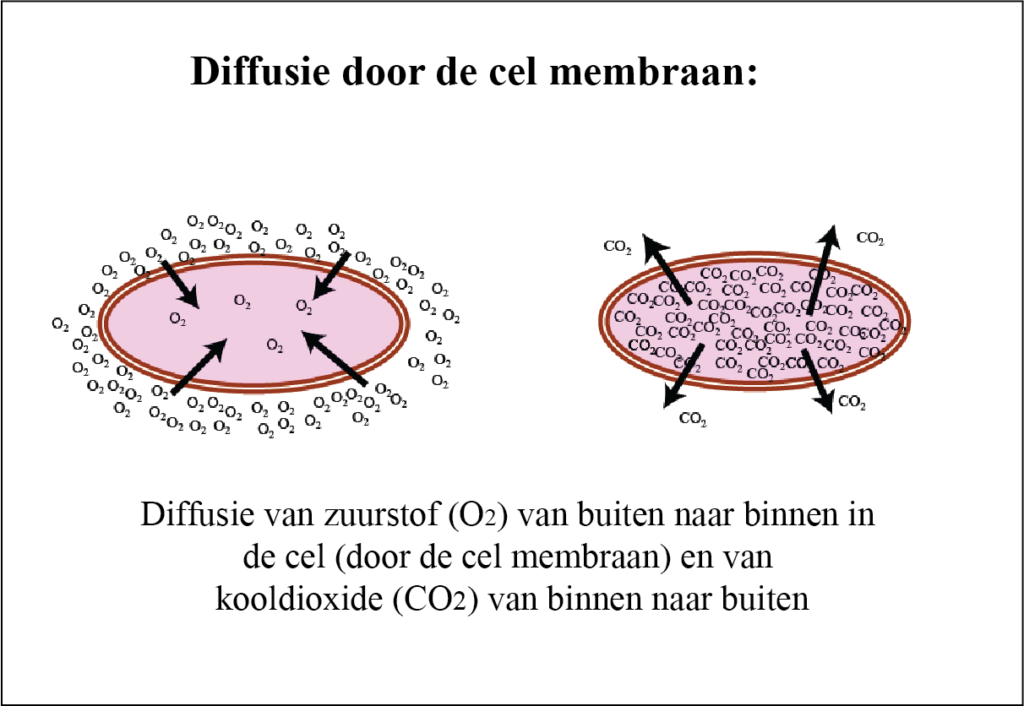
Zo kan bijvoorbeeld zuurstof, opgelost in water, gemakkelijk het membraan passeren. Gewoonlijk is de zuurstofconcentratie buiten de cel hoger dan binnen de cel (omdat deze door de cel wordt gebruikt).
3.
Dus, als er een concentratieverschil is voor zuurstof, dan zal zuurstof door het membraan diffunderen en zichzelf automatisch in de cel transporteren. Dit vereist geen energie.
4.
Hetzelfde gebeurt in de tegenovergestelde richting met het verbrandingsproduct van zuurstof; kooldioxide (CO2). Dit molecuul wordt gevormd in de cel (door zuurstof om te zetten) en diffundeert uit de cel naar de extracellulaire ruimte.
1.
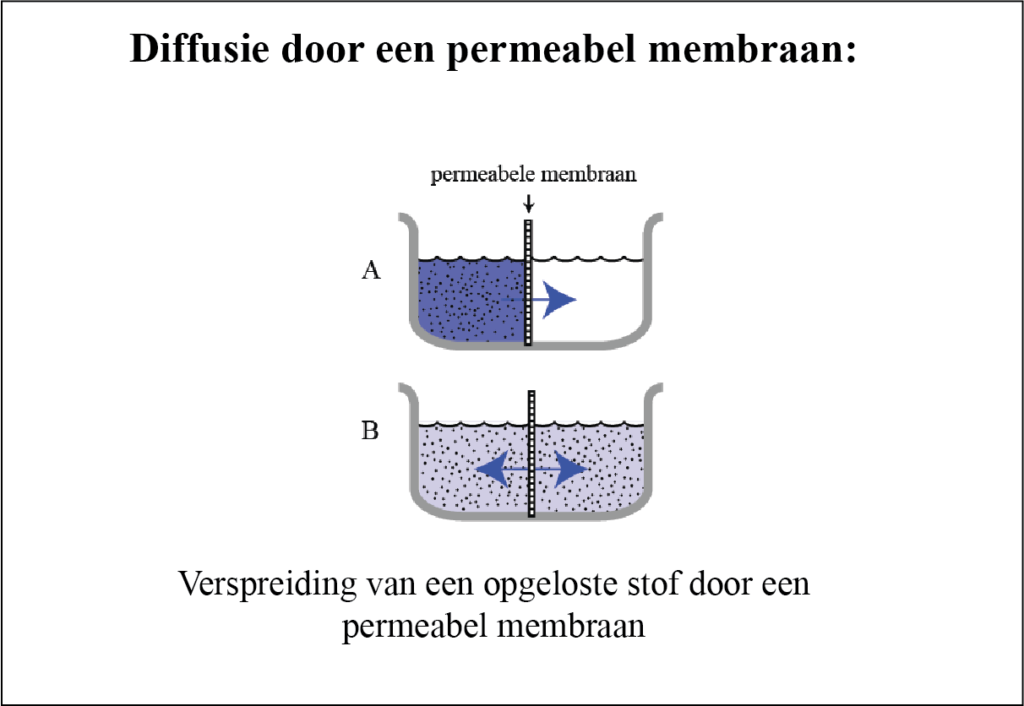
In dit diagram wordt een beker door tweeën gedeeld door een membraan. Aan de linkerkant is een opgeloste stof (blauw) aan de vloeistof toegevoegd.
2.
Omdat de moleculen door het membraan heen kunnen gaan, zullen steeds meer moleculen het membraan naar de andere kant passeren (door hun kinetische energie).
3.
Uiteindelijk, als je lang genoeg wacht, zal de concentratie rechts van het membraan hetzelfde worden als de linker concentratie (lichtblauw in beide helften).
Uiteindelijk, als je lang genoeg wacht, zal de concentratie rechts van het membraan hetzelfde worden als de linker concentratie (lichtblauw in beide helften).
4.
De factoren die de diffusiesnelheid bepalen zijn:
De factoren die de diffusiesnelheid bepalen zijn:
- temperatuur
- het verschil in concentratie
- de diffusieafstand
- de grootte van het diffusiegebied (=membraan)
5.
Verhoging van de temperatuur zal de bewegingen van de deeltjes verhogen en dit zal de diffusie versnellen.
6.
Hoe groter het concentratieverschil, hoe sneller de diffusie plaatsvindt.
7.
Hoe groter de afstand tussen de twee compartimenten (dikkere membraan), hoe langer de diffusie zal plaatsvinden. Aan de andere kant, hoe groter het permeabel membraan, hoe sneller de diffusie dan plaatsvindt.
8.
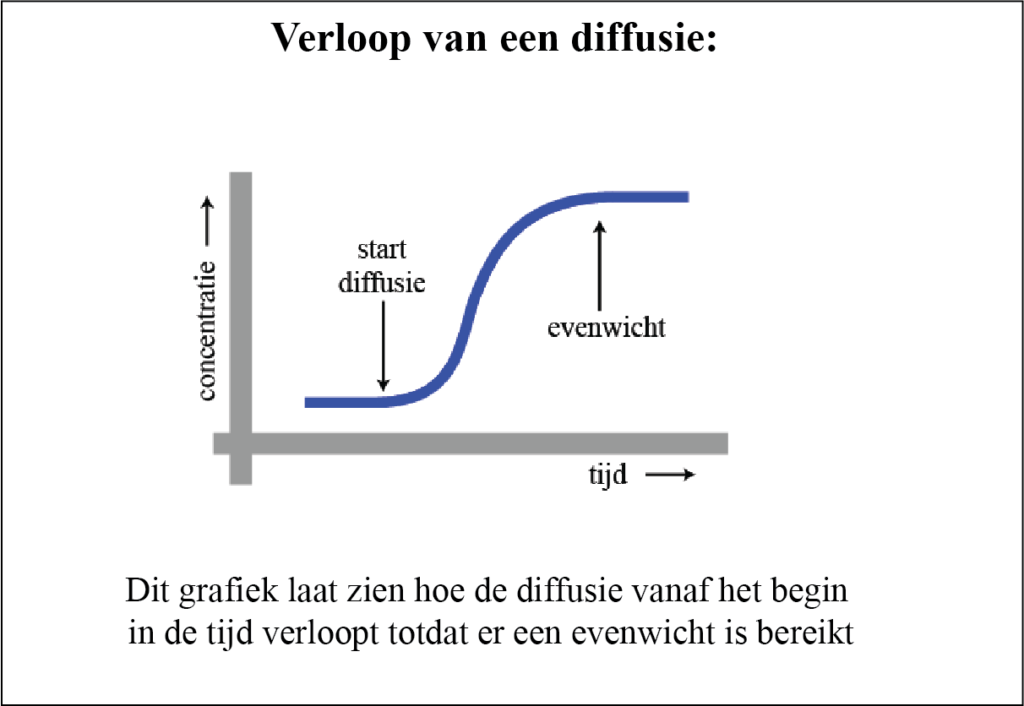
De grafiek toont wat er gebeurt wanneer de diffusie wordt gestart. Na enige tijd is de concentratie aan beide zijden gelijk geworden en zal de netto diffusie worden gestopt (waarom ‘netto’?)
1.
Dit type diffusie wordt uitgevoerd door speciale eiwitten die zich in het membraan van de cel bevinden.
2.
Het membraan is dus voor deze moleculen niet permeabel. Maar de moleculen worden door het membraan getransporteerd door deze speciale ‘dragers’.
Het membraan is dus voor deze moleculen niet permeabel. Maar de moleculen worden door het membraan getransporteerd door deze speciale ‘dragers’.
3.
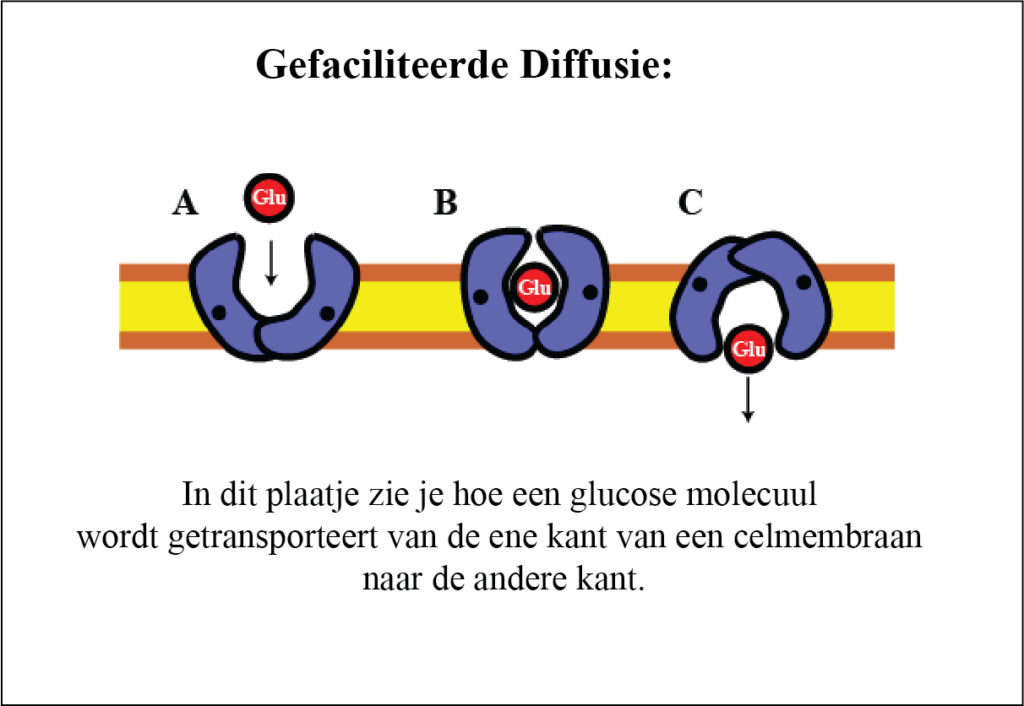
Een beroemd voorbeeld van gefaciliteerde diffusie is het transport van glucose (= suiker) naar de cel.
4.
Het glucosemolecuul is te groot om door het membraan te diffunderen.
5.
Maar er is een speciale drager in het membraan die glucose kan transporteren, vrij van energie (‘gratis’!).
6.
Deze drager is specifiek voor glucose; het kan niets anders vervoeren dan deze suiker.
7.
De vervoerder kan in beide richtingen transporteren; in of uit de cel, afhankelijk van de concentratiegradiënt voor glucose.
8.
Maar meestal wordt glucose gemetaboliseerd (=verbruikt) in de cel, zodat de concentratie binnenin lager is, dus het transport is meestal van buiten de cel naar binnen.
1.
Wanneer een glucose molecule in contact komt met deze drager, zal de glucose zich koppelen (= hechten) aan de drager.
2.
Deze koppeling zal de vorm (= de configuratie) van de drager veranderen.
3.
Deze configuratiewijziging maakt het mogelijk dat de glucose naar de andere kant van het membraan ‘diffundeert’.
4.
Zodra de glucose de andere kant van de drager heeft bereikt, wordt het vrijgegeven in de cel en is de drager vrij om een volgende glucosemolecuul te transporteren.
Zodra de glucose de andere kant van de drager heeft bereikt, wordt het vrijgegeven in de cel en is de drager vrij om een volgende glucosemolecuul te transporteren.
1.
Overeenkomsten:
- geen energie vereist
- concentratie afhankelijk
- bi-directioneel
2.
Verschillen:
Verschillen:
- verzadiging
- specificiteit
3.
De overeenkomsten zijn duidelijk als je diffusie hebt bestudeerd (bi-directioneel betekent dat het molecuul beide kanten op kan; in of uit de cel)
4.
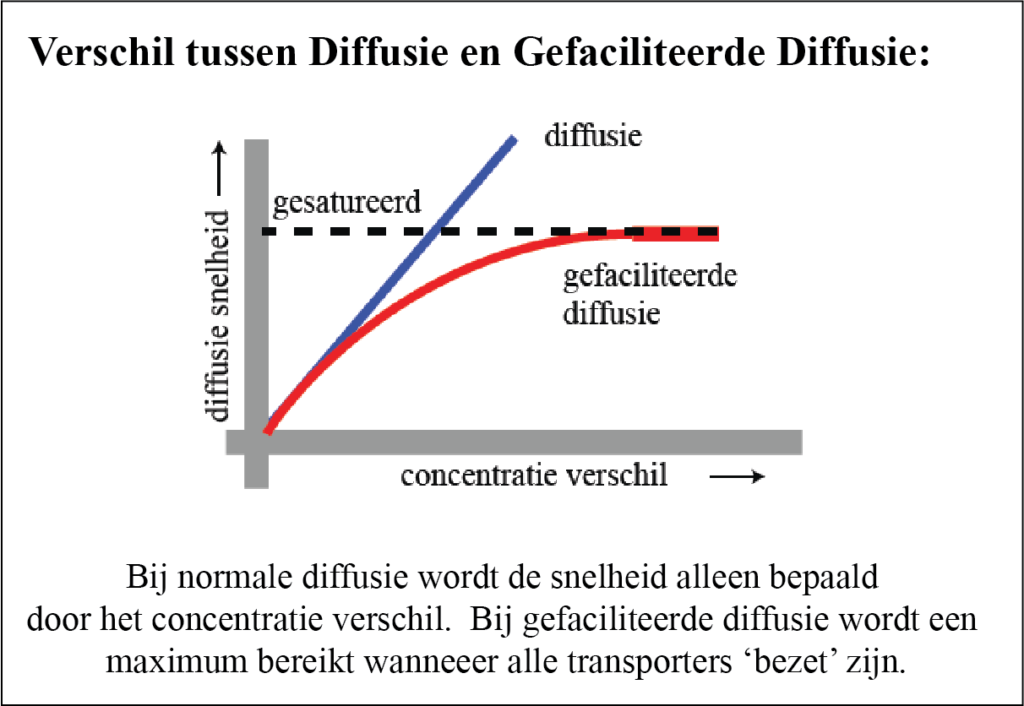
Verzadiging betekent dat er een maximum is voor de hoeveelheid die kan worden getransporteerd. Dit wordt bereikt wanneer alle beschikbare dragermoleculen bezet zijn.
Verzadiging betekent dat er een maximum is voor de hoeveelheid die kan worden getransporteerd. Dit wordt bereikt wanneer alle beschikbare dragermoleculen bezet zijn.
5.
Bij normale diffusie is er geen verzadiging en kan het proces zo lang mogelijk doorgaan, zolang er een concentratiegradiënt is.
6.
Specificiteit betekent dat een bepaalde drager alleen een bepaald molecuul, zoals glucose, kan vervoeren en niet iets anders.
7.
Voorbeeld van gefaciliteerde diffusie is het transport van glucose, zoals besproken, dat in wezen in alle lichaamscellen plaatsvindt, maar vooral in de hersenen. Ook aminozuren kunnen op deze manier door het celmembraan worden getransporteerd.
8.
Een ander voorbeeld van gefaciliteerde diffusie treedt op in de nier wanneer natrium wordt geresorbeerd. Dit wordt ook gedaan door gefaciliteerde diffusie.
1.
Een speciaal type diffusie, dat ook géén energie vereist, is diffusie van water, een proces dat osmose wordt genoemd.
2.
Osmose vindt plaats over een membraan. Dit membraan is permeabel voor water (zoals gewoonlijk) maar NIET permeabel voor een opgeloste stof. We noemen dit een semipermeabel membraan (niet permeabel voor de opgeloste stof maar wel permeabel voor water).
3.
Als er in deze situatie een concentratie verschil is van de opgeloste stof, dan is er ook een concentratieverschil voor water.
4.
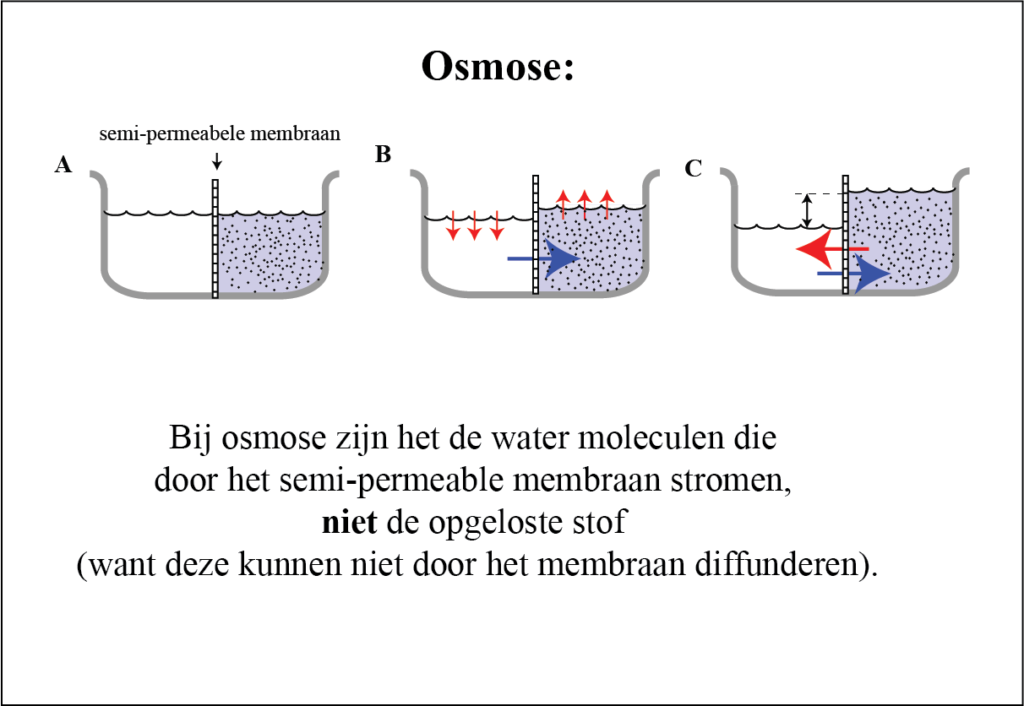
In het diagram (A) is er meer opgeloste stof (blauw) rechts dan links van het membraan. Maar deze opgeloste stof kan het membraan niet passeren, terwijl water dat wel kan.
5.
Omdat er aan de linkerkant van het membraan (een beetje) meer water is, is er een concentratieverschil voor water en stroomt watermoleculen naar de rechterkant (blauwe pijl).
Omdat er aan de linkerkant van het membraan (een beetje) meer water is, is er een concentratieverschil voor water en stroomt watermoleculen naar de rechterkant (blauwe pijl).
6.
Dit zal de hoeveelheid water aan de rechterkant vergroten! Zoals aangegeven in B, zal het waterniveau aan de rechterkant dan ook stijgen (en aan de linkerkant dalen).
7.
Zoals bij elke diffusie zal dit proces in principe doorgaan totdat het concentratieverschil over het membraan hetzelfde is geworden. Maar dit is niet altijd mogelijk.
8.
Zoals aangegeven in het diagram, zal de toename in water ook de kolom met water (en daarmee ook de druk) rechts van het membraan vergroten.
Zoals aangegeven in het diagram, zal de toename in water ook de kolom met water (en daarmee ook de druk) rechts van het membraan vergroten.
9.
Deze drukverhoging zorgt ervoor dat de watermoleculen weer naar links bewegen (rode pijl).
10.
Met andere woorden, een concentratie gradiënt naar rechts veroorzaakt een tegengestelde drukgradiënt naar links. Zodra de drukgradiënt gelijk is (maar tegengesteld) aan de concentratiegradiënt, is dit (osmose) systeem stabiel geworden (aangegeven door de blauwe en rode pijlen).
Met andere woorden, een concentratie gradiënt naar rechts veroorzaakt een tegengestelde drukgradiënt naar links. Zodra de drukgradiënt gelijk is (maar tegengesteld) aan de concentratiegradiënt, is dit (osmose) systeem stabiel geworden (aangegeven door de blauwe en rode pijlen).
1.
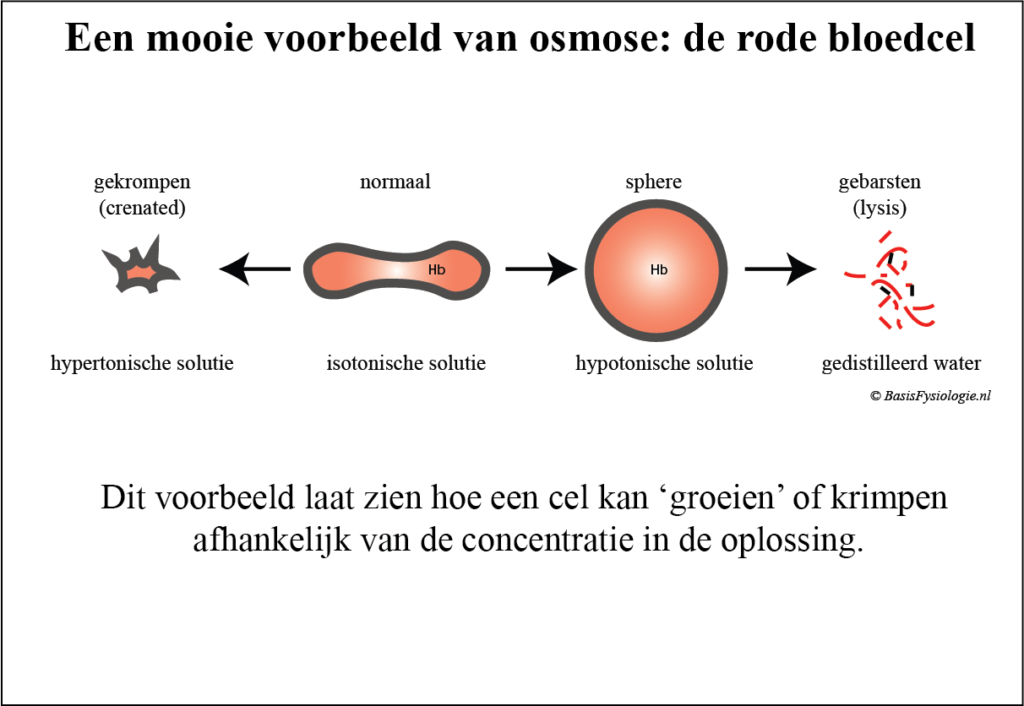
Een bekende demonstratie van de effecten van osmose is het gedrag van rode bloedcellen in een wateroplossing.
2.
Net als alle andere cellen hebben de rode bloedcellen (= erytrocyten) een plasmamembraan dat permeabel is voor water maar niet permeabel voor veel moleculen (zoals zout, hemoglobine enz.).
Net als alle andere cellen hebben de rode bloedcellen (= erytrocyten) een plasmamembraan dat permeabel is voor water maar niet permeabel voor veel moleculen (zoals zout, hemoglobine enz.).
3.
Als de rode bloedcel in een oplossing wordt geplaatst die minder niet-permeabele deeltjes bevat dan in de cel, dan zal er water in de cel komen; de cel zal dan ‘groeien’.
4.
De oplossing die minder niet-permeabele opgeloste stof bevat, wordt ‘hypotonisch’ genoemd. Als de oplossing dezelfde hoeveelheid opgeloste stof bevat, wordt de oplossing ‘isotonisch’ genoemd (iso = gelijk; tonisch = toon).
De oplossing die minder niet-permeabele opgeloste stof bevat, wordt ‘hypotonisch’ genoemd. Als de oplossing dezelfde hoeveelheid opgeloste stof bevat, wordt de oplossing ‘isotonisch’ genoemd (iso = gelijk; tonisch = toon).
5.
Als het verschil te groot is, bijvoorbeeld als er helemaal geen opgeloste stof in de omgeving is, kan de cel zichzelf opblazen, breken en barsten (= lysis).
6.
Het tegenovergestelde kan ook gebeuren. Als de rode bloedcel zich in een oplossing bevindt die te veel zout bevat (= hypertoon), dan zal water uit de cel bewegen; de rode bloedcel zal dan krimpen!
1.
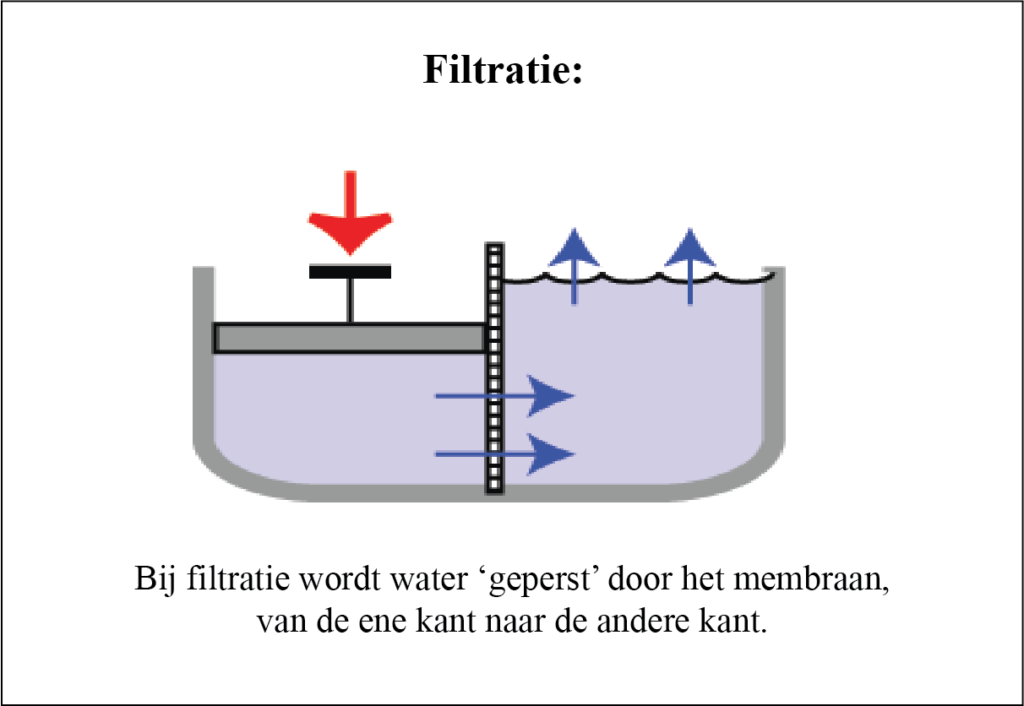
Bij filtratie is er in eerste instantie een drukverschil tussen de ene kant van de membraan en de andere kant.
2.
Vanwege dit drukverschil zal water stromen van het gebied van hoge druk naar dat van lage druk, ervan uitgaande dat de membraan waterdoorlatend is (wat meestal het geval is).
3.
Filtratie vindt plaats in veel delen van het lichaam, maar vooral bij het transport van plasma door capillairen, in de nieren (urinevorming) en in de longen.
B.4. Wat is kinetisch?
Kinetische energie (van het Griekse woord ‘Kinein’ = bewegen) is aanwezig in alle opgeloste deeltjes en moleculen. Deze energie zal de deeltjes de hele tijd ‘schudden’. De schudintensiteit neemt toe met hogere temperaturen en vertraagt bij lagere temperaturen. Het schudden stopt volledig bij het absolute nulpunt (o0 Kelvin = -273 oC = -459 oF).
Kinetische energie (van het Griekse woord ‘Kinein’ = bewegen) is aanwezig in alle opgeloste deeltjes en moleculen. Deze energie zal de deeltjes de hele tijd ‘schudden’. De schudintensiteit neemt toe met hogere temperaturen en vertraagt bij lagere temperaturen. Het schudden stopt volledig bij het absolute nulpunt (o0 Kelvin = -273 oC = -459 oF).
D.8. Waarom ‘netto’?
In werkelijkheid, omdat de moleculen nog steeds volgens hun kinetische energie bewegen, zullen sommige moleculen per ongeluk het membraan passeren en naar de andere kant bewegen. Maar andere moleculen die per ongeluk in de tegenovergestelde richting bewegen, zullen dit compenseren. Met andere woorden, de moleculen bewegen nog steeds naar links en naar rechts, maar het netto-effect is nul.
In werkelijkheid, omdat de moleculen nog steeds volgens hun kinetische energie bewegen, zullen sommige moleculen per ongeluk het membraan passeren en naar de andere kant bewegen. Maar andere moleculen die per ongeluk in de tegenovergestelde richting bewegen, zullen dit compenseren. Met andere woorden, de moleculen bewegen nog steeds naar links en naar rechts, maar het netto-effect is nul.